論文作者:鄒佳輝,指導教師:張文麗
所屬學院:藥學院,二級學科:藥劑學
01 導師說

在碩士學習階段,我認為最重要的是科研思維的培養(yǎng),而這種思維的培養(yǎng),首先需要學生具有濃厚的科研興趣和熱情。鄒佳輝同學是一個熱愛科研的學生,確定課題時,雖然也面臨過一些困難,但很快他憑借對課題濃厚的興趣,找到了問題的解決方向。這個課題最早的設計其實比較簡單,我們只是想突破常規(guī),探討微米載體的體內分布特性是否優(yōu)于納米載體。為了快速尋求答案,鄒佳輝將實驗安排得非常緊湊,二年級下學期未結束時,便做完了所有的體內實驗,比其他同學快了將近一年,在此過程中,他遇到很多困難,我問他有哪些困難需要幫助,但他的主觀能動性很強,從未因為這些問題影響過實驗進度,更多的時候是就方案設計等方面主動向我尋求幫助,我想這些也是他實驗做得快的主要原因。動物實驗結束后,我告訴他,目前的課題只是一個驗證性實驗,我們并沒有對結果進行深入的機制探討,你是否愿意做進一步嘗試?作為導師,我深知他的工作量已滿足碩士畢業(yè)要求,但令我意外的是,他欣然接受挑戰(zhàn),最終將這個課題做得非常完整,甚至在畢業(yè)后的暑假繼續(xù)完成了文章發(fā)表的相關工作。非常幸運能夠成為鄒佳輝的科研啟蒙導師,在他的身上,我看到了一個研究生應有的對科研的熱情,對未知的探索,以及拼搏向上的精神,相信在未來的科研道路上,他定能夠不斷突破自己,永攀高峰!
02 作者說

轉眼已是我來藥大第六個年頭,曾經(jīng)那個懵懂而又輕狂的少年,經(jīng)過不斷的磨礪,也已漸漸變得沉穩(wěn)。現(xiàn)如今回望,往日的點點滴滴仍歷歷在目。非常感謝張文麗老師給我的機會,讓我能夠從徐州醫(yī)科大學來到向往的藥大攻讀碩士研究生。最開始面對仿生藥物遞送系統(tǒng)這個全新的領域,讓我有些手足無措。當一個接一個的失敗接踵而至時,一度讓我想要放棄。是張文麗老師一直的鼓勵與幫助,讓我重拾信心;是朋友們一直的支持,讓我奮勇向前。在老師的指引下,讓我對科研學習有了更深刻的認識,培養(yǎng)了我對科學問題的正確思考方式。也是老師的信任,相信我能突破自我,能夠攻克這個困難的課題,在無數(shù)的不確定下,仍然支持我的想法。尤其在探索這種新的課題過程中,老師不斷地糾正我的錯誤觀點和不合理的設計,讓我在正確的方向上深入地挖掘。老師的平日里的關心以及課題組融洽的氛圍,也讓我內心充滿了溫暖,在荊棘的道路上不會孤單。當然,正是一路上遇到的種種挫折,讓我面對學習中的困難有了沉穩(wěn)的心態(tài)。
碩士的學習生活中,老師不僅指引了我的未來規(guī)劃,也塑造了我的人生觀。在不斷探索的過程中,讓我擁有了面對未知的勇氣和迎接挑戰(zhàn)的決心。無論是何科學問題,選擇了就不能放棄。只要我們堅持不懈,每一次微小的進步都有可能會為疾病的攻克添磚加瓦。作為一名藥學生,我為自己的選擇感到驕傲。盡管前路漫漫,但每一個實驗、每一篇論文、每一次失敗與成功,都是這段旅程中不可或缺的一部分。科學探索的魅力就在于它的無限可能,而正是這些可能性,讓我對未來充滿期待。習總書記教導我們青年人需要立大志、明大德、成大才、擔大任,要不忘初心、砥礪前行。未來我將繼續(xù)秉持著“精業(yè)濟群”的精神,在科學的道路上不斷探索,為患者點燃希望,為人類健康保駕護航。
03碩士論文簡介
長久以來惡性腫瘤嚴重威脅著人類的生命健康,是困擾世界臨床診療的一大難題。近幾十年來,基于增強滲透及滯留(EPR)效應設計的納米藥物遞送系統(tǒng)被廣泛研究和應用,以提高載體在腫瘤組織中的分布和蓄積。然而,研究表明,由于靶向選擇性不足,只有不到1 %的納米顆粒能夠有效到達腫瘤組織,且納米藥物遞送系統(tǒng)的臨床治療效果改善并不顯著。尤其在體內肝臟等正常組織器官中,納米藥物載體易于通過較大的血管內皮間隙外滲并產(chǎn)生蓄積,不可避免地造成毒副作用。同時在循環(huán)系統(tǒng)中,NDDS易于受到網(wǎng)狀內皮系統(tǒng)(RES)的吞噬和清除,導致體內循環(huán)時間較短。受“天然偽裝”的啟發(fā),仿生納米藥物遞送系統(tǒng)引起了研究者們的廣泛關注。通過將生物質膜與納米顆粒進行組裝和修飾能夠顯著改善NDDS的體內命運,但這種基于膜包裹的修飾仍然無法改善由納米尺寸效應引起的正常組織蓄積所帶來的全身性分布毒性。
為了提高腫瘤靶向和穿透,同時兼顧載體的體內安全性,本研究打破了傳統(tǒng)仿生藥物遞送系統(tǒng)設計的桎梏,探索構建了一種無內涵顆粒化的微米級血小板“鬼影”載體,并通過“低滲-透析”法包封具有光熱腫瘤殺傷作用的中空金納米粒,構建了具有酸響應的級聯(lián)仿生血小板“微膠囊”(PG@HGNs)。PG@HGNs能夠借助PGs完整微米級細胞結構及表面膜相關蛋白CD47和P-選擇素,顯著延長體內循環(huán)時間并提高腫瘤靶向作用。同時微米級的尺寸效應能夠限制載體在正常組織中的蓄積,提高體內安全性。靶向腫瘤部位后,PG@HGNs響應腫瘤酸性微環(huán)境,通過膜糖蛋白Ib的響應性調節(jié)提高膜流動性以快速釋放包封的納米級HGNs實現(xiàn)粒徑切換,并進一步借助EPR效應深入穿透腫瘤組織,在近紅外激光的激發(fā)下產(chǎn)生強大的光熱作用以有效殺傷腫瘤。
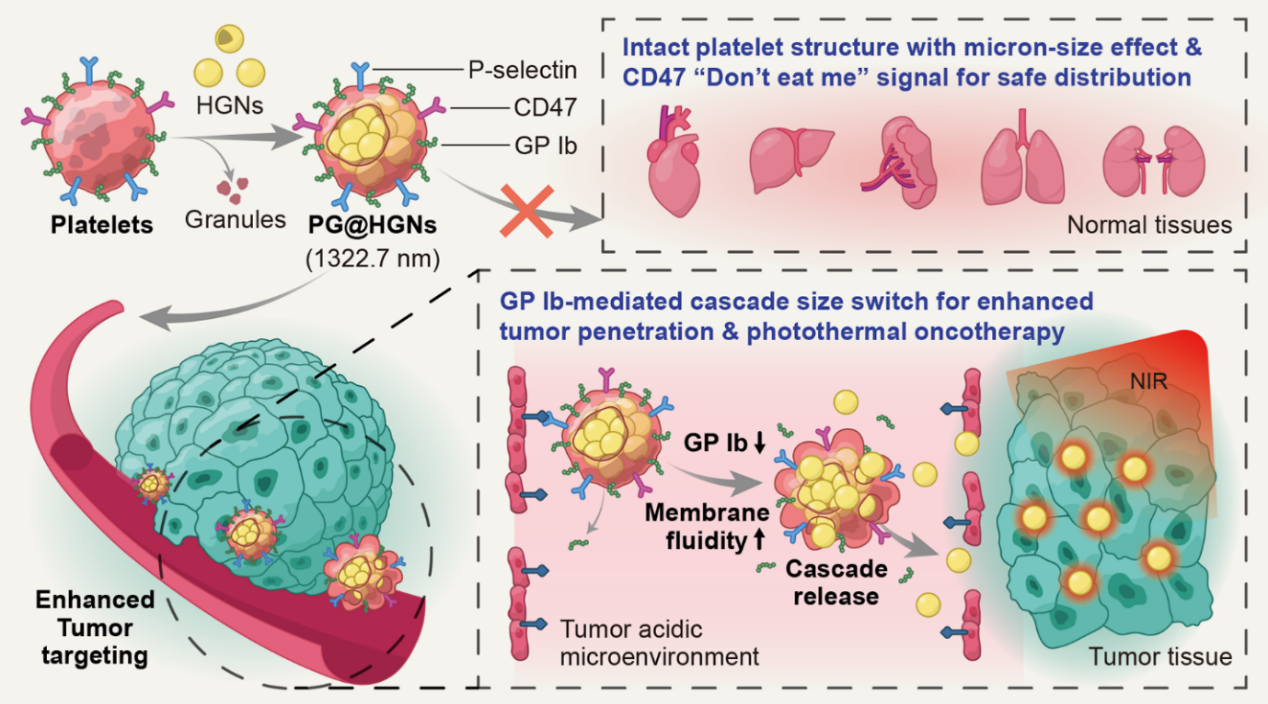
級聯(lián)仿生血小板“微膠囊”的構建及其光熱抗腫瘤療治療機制
學術成果
課題圍繞如何實現(xiàn)腫瘤特異性靶向遞送并提高體內分布安全性和腫瘤穿透性的問題,探索性構建了具有腫瘤酸性微環(huán)境響應特性的微米-納米粒徑可切換的級聯(lián)仿生藥物遞送系統(tǒng)(PG@HGNs)。采用具有完整細胞結構的微米級血小板“鬼影”提高了復合載體的生物相容性,延長載體體內循環(huán)時間并提高靶向效率。通過體外釋放、熒光偏振和Western blot實驗成功驗證了PG@HGNs具有酸敏感性調節(jié)的功能,并通過基于分子機制的深入研究發(fā)現(xiàn),這種酸響應性釋放主要是由于血小板在酸性環(huán)境中,膜表面參與細胞骨架構成的膜糖蛋白Ib快速流失,導致血小板膜流動性顯著升高,促進內部包封的HGNs快速觸發(fā)式響應釋放,實現(xiàn)微米-納米的粒徑切換。內部包封的納米級的HGNs經(jīng)篩選合成后具有合適的粒徑,通過EPR效應能夠深入穿透腫瘤組織并在腫瘤中有效蓄積。在近紅外激光的激發(fā)下產(chǎn)生強大的光熱作用以有效殺傷腫瘤。綜上,通過PG@HGNs能夠提高載體的腫瘤靶向性和體內分布安全性。
[1] Zou, Jiahui, Jianhua He, Xiaobo Wang, Yajie Wang, Chenchen Wu, Mengya Shi, Hulin Jiang, Zimei Wu, Jianping Liu, and Wenli Zhang. Glycoprotein Ib-regulated micro platelet ghost for biosafe distribution and photothermal oncotherapy. Journal of Controlled Release, 351 (2022): 341-360.
[2] Su, Jiajia#, Chenchen Wu#, Jiahui Zou#, Xinqiuyue Wang, Kaiyun Yang, Jianping Liu, Zimei Wu, and Wenli Zhang. Fine-tuning of liposome integrity for differentiated transcytosis and enhanced antitumor efficacy. Journal of Controlled Release, 372 (2024): 69-84.
[3] Liu, Xinyue, Yajie Wang, Jiahui Zou, Hui Wang, Xuechun Li, Ying Huang, Enshi Hu, Danyi Quan, Jianping Liu, Wenli Zhang. Quasi-opsonin conjugated lipase-sensitive micelles activate macrophages against facultative intracellular bacterial infection. Journal of Materials Chemistry B, 11, 4 (2023): 865-878.
[4] Wu, Chenchen, Zhiyu Wang, Xiaobo Wang, Jiahui Zou, Zimei Wu, Jianping Liu, and Wenli Zhang. Morphology/interstitial fluid pressure-tunable nanopomegranate designed by alteration of membrane fluidity under tumor enzyme and PEGylation. Molecular pharmaceutics, 18, 5 (2021): 2039-2052.

