論文作者:劉定康,指導(dǎo)教師:高向東
所屬學(xué)院:生命科學(xué)與技術(shù)學(xué)院,二級(jí)學(xué)科:生物學(xué)
01 導(dǎo)師說

本課題源于中國(guó)藥科大學(xué)“雙一流”建設(shè)項(xiàng)目與江蘇省研究生科研與實(shí)踐創(chuàng)新計(jì)劃,旨在探索并設(shè)計(jì)針對(duì)腫瘤多藥耐藥(MDR)的有效方法。在以往失敗的MDR臨床案例中,研究者們往往只是針對(duì)某一種ABC轉(zhuǎn)運(yùn)體進(jìn)行抑制劑的開發(fā)。然而,耐藥過程中通常都有多種ABC轉(zhuǎn)運(yùn)體參與,相互之間還存在補(bǔ)償性上調(diào)的現(xiàn)象,因此理想的ABC轉(zhuǎn)運(yùn)體抑制劑需要廣譜的抑制活性。本課題采用了一種新型策略,通過破壞耐藥腫瘤細(xì)胞的線粒體功能來克服多藥耐藥性。以具有破壞線粒體功能的生物活性肽R8-KLA為模式分子,與我們前期開發(fā)的一種人工定向設(shè)計(jì)的聚多肽PsTag進(jìn)行融合,構(gòu)建了一種長(zhǎng)效、具有腫瘤靶向和響應(yīng)釋放的新型融合蛋白PAK。在隨后的研究中,我們證實(shí)PAK可通過靶向損傷腫瘤細(xì)胞線粒體,降低胞內(nèi)ATP水平,有效提高M(jìn)DR腫瘤細(xì)胞對(duì)化療藥物的攝取和敏感性。由于需要ATP提供能量是所有ABC轉(zhuǎn)運(yùn)體發(fā)揮功能的共同前提,因此PAK在克服ABC轉(zhuǎn)運(yùn)體導(dǎo)致的腫瘤MDR中具有廣泛的適用性。目前,融合蛋白PAK的設(shè)計(jì)、制備及其應(yīng)用已申請(qǐng)中國(guó)國(guó)家發(fā)明專利(ZL201811632324.1)。此外,PAK可在原核表達(dá)系統(tǒng)中表達(dá),產(chǎn)物組分均一,易于規(guī)模化制備及質(zhì)量控制,具有良好的臨床應(yīng)用前景。
02 作者說

盡管近年來的生物療法發(fā)展十分迅速,化療仍然是許多類型癌癥的最有效療法。不幸的是,大多數(shù)接受化療的癌癥患者都會(huì)產(chǎn)生多藥耐藥(MDR)。持續(xù)的研究發(fā)現(xiàn),幾乎每種有效抗癌藥,甚至包括新開發(fā)的藥物,如廣譜化療藥物和酪氨酸激酶抑制劑,都存在耐藥的問題。針對(duì)該挑戰(zhàn),我們嘗試從三個(gè)方面進(jìn)行探索:
首先,我們?yōu)槟退帉?shí)體瘤治療提供了新的藥物候選分子——融合蛋白PAK。針對(duì)耐藥過程中ABC轉(zhuǎn)運(yùn)體參與廣泛并存在補(bǔ)償性上調(diào)的問題,PAK能夠通過靶向損傷腫瘤細(xì)胞線粒體,降低胞內(nèi)ATP水平,有效提升MDR腫瘤細(xì)胞對(duì)化療藥物的攝取和敏感性。由于ABC轉(zhuǎn)運(yùn)體發(fā)揮功能的前提是需要ATP提供能量,因此PAK在克服ABC轉(zhuǎn)運(yùn)體導(dǎo)致的腫瘤MDR方面具有一定的通用性。
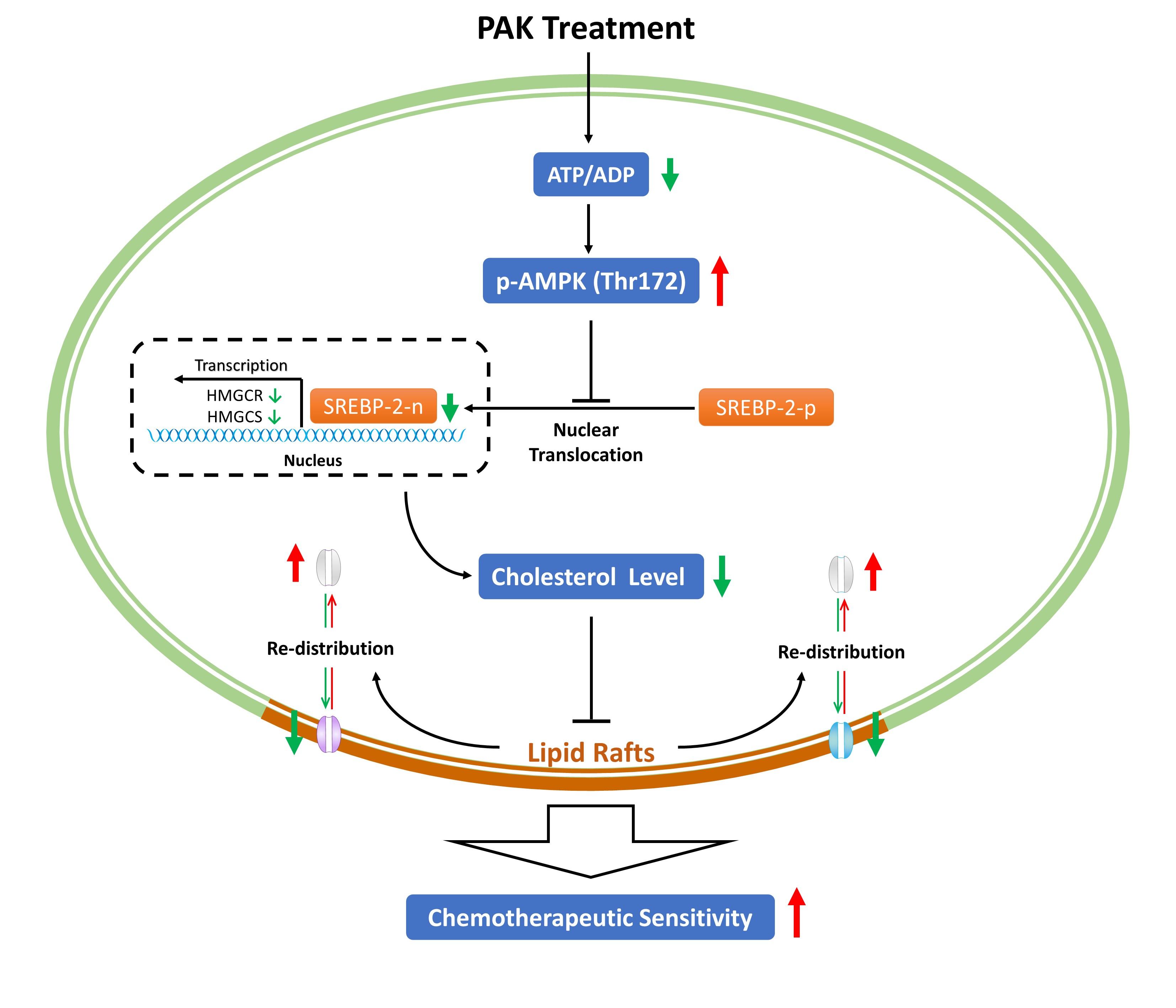
其次,本研究為克服腫瘤多藥耐藥提供了新的研究思路。耐藥癌細(xì)胞相比敏感癌細(xì)胞更少依賴糖酵解途徑獲得能量,而主要依賴線粒體氧化磷酸化(OxPhos)來維持較高的ATP水平。我們發(fā)現(xiàn)PAK不僅能夠抑制線粒體OxPhos降低ATP水平,還能改變ABC轉(zhuǎn)運(yùn)體在脂筏上的定位。這一發(fā)現(xiàn)揭示了一種耐藥逆轉(zhuǎn)模式,即通過藥物破壞脂筏,降低ABC轉(zhuǎn)運(yùn)體在細(xì)胞膜上的分布,從而增強(qiáng)耐藥細(xì)胞對(duì)化療的敏感性。
最后,本研究提供了一種抗腫瘤多肽靶向遞送的方法。雖然生物活性肽是針對(duì)內(nèi)源性靶點(diǎn)的天然候選藥物,但其體內(nèi)半衰期短的問題限制了其臨床應(yīng)用。我們成功設(shè)計(jì)了一種融合蛋白PAK,將R8-KLA遞送至腫瘤細(xì)胞內(nèi)發(fā)揮其線粒體損傷活性。這一方法不僅為R8-KLA的遞送提供了解決方案,還為其他抗腫瘤多肽的靶向遞送提供了借鑒。但是,本論文也還存在一些不足之處。比如,融合蛋白PAK的產(chǎn)量較低,難以滿足潛在的工業(yè)化需求。同時(shí),樣品保存條件、短期及長(zhǎng)期保存穩(wěn)定性等也需要進(jìn)一步研究。其次,膽固醇調(diào)控脂筏的具體機(jī)制尚需進(jìn)一步探索。雖然本研究證明了PAK通過下調(diào)膽固醇水平提高了MDR腫瘤細(xì)胞的化療敏感性,并確認(rèn)了膽固醇與ABC轉(zhuǎn)運(yùn)體再分布之間的調(diào)控關(guān)系,但膽固醇如何參與脂筏結(jié)構(gòu)的維持并導(dǎo)致ABC轉(zhuǎn)運(yùn)體在脂筏上定位減少的具體機(jī)制尚不明確,有待進(jìn)一步深入研究。
總之,我們發(fā)現(xiàn)PAK通過靶向線粒體抑制了細(xì)胞內(nèi)膽固醇水平,導(dǎo)致MDR相關(guān)的ABC轉(zhuǎn)運(yùn)蛋白在脂筏區(qū)和細(xì)胞質(zhì)之間重新分布。這些結(jié)果是一個(gè)激動(dòng)人心的開始,證明了靶向線粒體在克服MDR方面的有效性。
03 博士論文簡(jiǎn)介
多藥耐藥(MDR)是腫瘤治療的主要障礙。研究表明,腫瘤細(xì)胞的高能態(tài)與耐藥性密切相關(guān)。因此,通過藥物破壞線粒體可能是一種克服MDR的有效策略。本研究基于前期開發(fā)的聚多肽PsTag融合技術(shù)和腫瘤微環(huán)境的特點(diǎn),提出構(gòu)建“一種將線粒體損傷肽靶向遞送至MDR腫瘤細(xì)胞以提高化療敏感性”的設(shè)想。為了測(cè)試這一設(shè)想,我們采用一種經(jīng)典的線粒體損傷肽R8-KLA作為我們的模式多肽,設(shè)計(jì)了一種融合蛋白PAK(PsTag-ACPP-KLA)。完整序列含有以下三個(gè)部分:216個(gè)氨基酸的PsTag聚多肽序列,可激活的細(xì)胞穿透肽(ACPP),以及具有線粒體損傷作用的多肽KLA。首先,我們構(gòu)建了融合蛋白PAK的原核表達(dá)菌株,并對(duì)目的蛋白進(jìn)行了誘導(dǎo)表達(dá)和純化,成功得到了HPLC純度大于95%的目的蛋白。進(jìn)一步MMP2酶切鑒定結(jié)果顯示,PAK在37℃處理4小時(shí)即可被MMP2完全消化。PAK還表現(xiàn)出良好的血清穩(wěn)定性,且未檢測(cè)出溶血毒性和免疫原性。進(jìn)一步,PAK通過降低線粒體膜電位、激活線粒體凋亡通路的方式產(chǎn)生細(xì)胞毒性。MTT、克隆形成和腫瘤成球試驗(yàn)的結(jié)果共同顯示,PAK可以有效提高M(jìn)DR腫瘤細(xì)胞的化療敏感性。機(jī)制上,PAK提高了胞內(nèi)ROS的水平,降低了胞內(nèi)NADH和ATP的水平。同時(shí),PAK可以有效地內(nèi)化到MCF7/Dox細(xì)胞中,且與線粒體高度共定位。進(jìn)一步結(jié)果顯示,PAK通過AMPK/SREBP2軸下調(diào)了胞內(nèi)膽固醇的水平,從而誘導(dǎo)了ABC轉(zhuǎn)運(yùn)體從脂筏到胞內(nèi)的轉(zhuǎn)移。綜上,我們提出了一種通過蛋白融合技術(shù)向腫瘤靶向遞送線粒體損傷肽的策略,并基于該策略構(gòu)建了融合蛋白PAK。同時(shí),揭示了一種耐藥逆轉(zhuǎn)模式:線粒體損傷通過破壞脂筏,增強(qiáng)耐藥癌細(xì)胞對(duì)化療的敏感性,表明線粒體可能是逆轉(zhuǎn)惡性腫瘤MDR的潛在靶點(diǎn)。
學(xué)術(shù)成果
1. Liu Dingkang#, Rong Haibo#, Chen Ye, Wang Qun, Qian Sijia, Ji Yue, Yao Wenbing*, Yin Jun*, Gao Xiangdong*. Targeted Disruption of Mitochondria Potently Reverses Multidrug Resistance in Cancer Therapy[J]. British Journal of Pharmacology, 2022, 179(13): 3346-3362. DOI: 10.1111/bph.15801.
2. Liu Dingkang#, Chen Ye#, Wang Qun, Ji Yue, Bao Lichen, Yao Wenbing*, Gao Xiangdong*, Yin Jun*. Tailored Protein-Conjugated DNA Nanoplatform for Synergistic Cancer Therapy[J]. Journal of Controlled Release, 2022, 346:250-259. DOI: 10.1016/j.jconrel.2022.04.022.
3. Yin Jun#, Liu Dingkang#, Bao Lichen, Wang Qun, Chen Ye, Hou Shan, Yue Yali, Yao Wenbing*, Gao Xiangdong*. Tumor targeting and microenvironment-responsive multifunctional fusion protein for pro-apoptotic peptide delivery[J]. Cancer Letters, 2019, 452: 38-50. DOI: 10.1016/j.canlet.2019.03.016.
4. Wang Qun, Yang Yifan, Liu Dingkang, Ji Yue, Gao Xiangdong*, Yin Jun*, Yao Wenbing*. Cytosolic protein delivery for intracellular antigen targeting using supercharged polypeptide delivery platform[J]. Nano Letters, 2021, 21 (14): 6022-6030. DOI: 10.1021/acs.nanolett. 1c01190.
5. Yin Jun#, Hou Shan#, Wang Qun, Bao Lichen, Liu Dingkang, Yue Yali, Yao Wenbing*, Gao Xiangdong*. Microenvironment-responsive delivery of the cas9 RNA-guided endonuclease for efficient genome editing[J]. Bioconjugate Chemistry, 2019, 30 (3): 898-906. DOI: 10.1021/acs.bioconjchem.9b00022.

